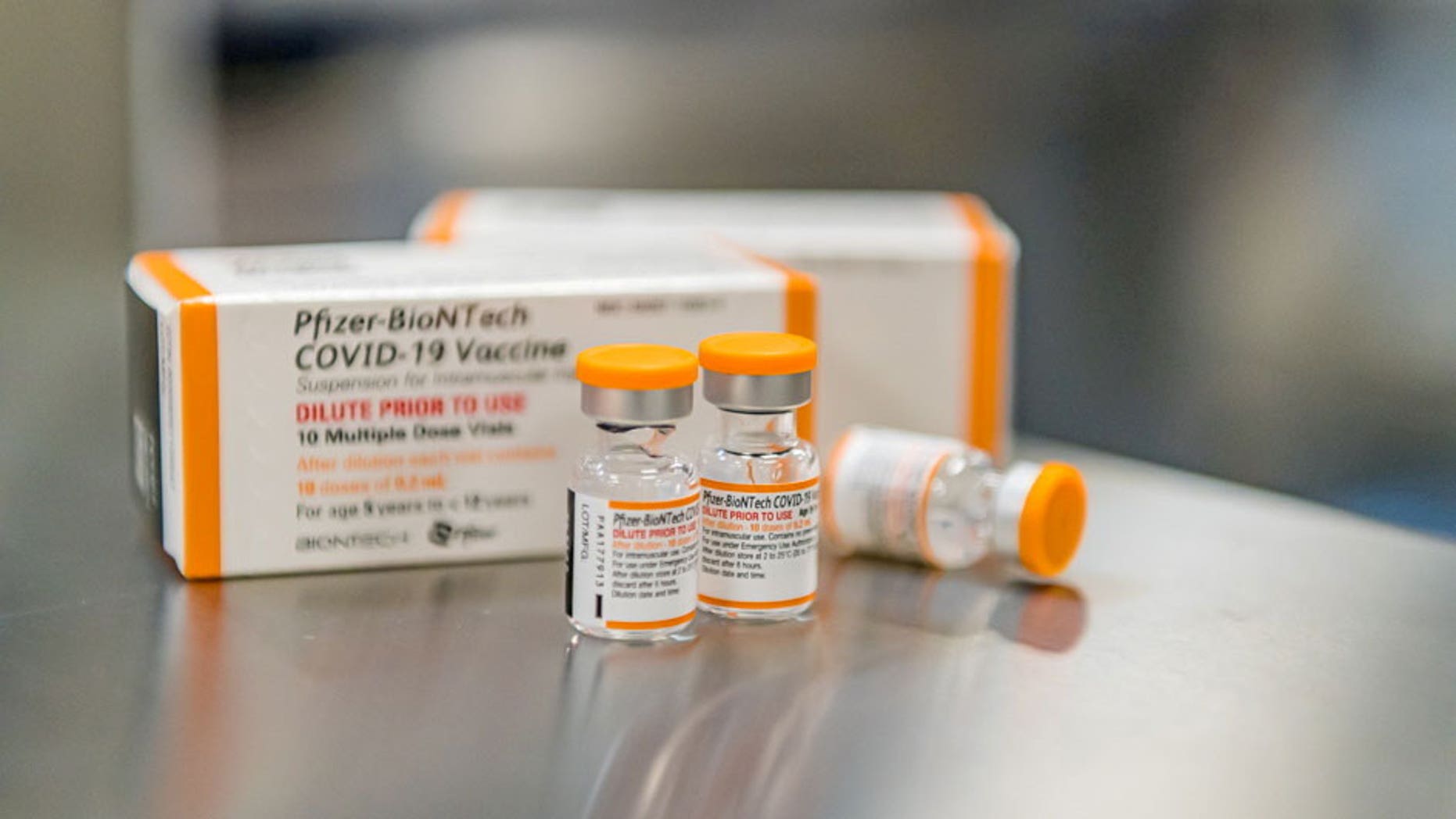
据《卫报》近日报道,在美国联邦食品和药物管理局(FDA)上周推迟批准辉瑞生物技术公司(Pfizer-BioNTech)针对5岁以下儿童的COVID-19疫苗后,家长们强烈呼吁将其用于非适应症使用。
美国儿科学会(AAP) 2021年主席李·萨维奥·比尔斯博士在一份声明中表示,去年夏天,美国儿科学会(AAP)建议12岁以下儿童不要超说明书用药。
“对年轻人来说,剂量可能不同。美国儿科学会建议,在获得FDA批准之前,不要给12岁以下的儿童接种疫苗。”
据报道,Moderna疫苗被批准用于18岁及以上的成人,而辉瑞- biontech疫苗被批准用于16岁及以上的成人,但针对年轻患者的疫苗仍在紧急使用授权中。
报告说,198彩票注册账户安全可靠198彩平台,198彩票平台采用最新国际加密系统,保证玩家的个人隐私是不会泄露的,当卫生保健提供者签署一项管理疫苗的协议时,他们同意不为非授权适应症(如超适应症使用)提供疫苗。
儿科传染病专家、美国儿科学会传染病委员会副主席Sean O’leary博士最近在接受《卫报》采访时表示:“如果疫苗提供者向这些儿童提供疫苗,他们可能会失去疫苗提供者的地位。”
据《卫报》报道,批准用于5至11岁儿童的10微克疫苗尚未在更小的儿童身上进行研究,辉瑞生物技术公司的儿科试验中,儿童接受3微克剂量的疫苗,因此,如果5岁以下的儿童接受更高剂量的疫苗,可能会产生更多的副作用。
但这篇论文指出,一些家长和医生认为,临床试验已经证明3微克剂量对幼儿是安全的。
德国家庭医生沃尔夫冈·冯·迈斯纳博士说:“我没有看到4岁和5岁的孩子有什么不同,除了年龄——免疫系统发挥的作用是一样的。”
但是Pfizer-BioNTech之后发现了ο变种感染导致更高的速度比先前记录在年轻患者的临床试验,他们要求延迟变异的授权,因为躲避的能力提供的免疫剂治疗系列疫苗,据《纽约时报》。
本文指出,临床试验数据显示,12月两岁之间的儿童和四只产生60%的抗体反应的抗体反应相比,年长的青少年和年轻的成年人,一组作为基准来记录疫苗的有效性。
相比之下,6个月到2岁的儿童产生了一种抗体保护,达到了研究的目标,没有安全问题,但这些儿童使用的剂量是12岁及12岁以上儿童的十分之一,《纽约时报》补充说。
然而,在德国,冯•迈斯纳已经2500岁的儿童疫苗接种六个月到五岁,因为即使疫苗不批准5岁以下儿童,没有限制其标示外使用在美国,据《卫报》。
“我不明白为什么我不应该保护小孩子,”他说。但他警告说,在使用未经批准的超说明书使用疫苗之前,告知父母其风险是很重要的。
“他们需要理解,198才手机APP198彩票平台开户开发人员近期宣布,新版手机版将在下月全新上线并免费提供下载网址,欢迎各位198彩票注册网民来试验。,然后他们需要做出决定,”他补充说。
•冯•迈斯纳说,扩大疫苗一个标示外使用在美国将给予额外的保护家庭,有些人变得如此绝望,谎报年龄儿童,这样孩子可以符合他们的标准,但这是由专家强烈建议反对,/报告。
这篇论文指出,让更多儿童接种疫苗的另一种选择可能是,如果辉瑞生物技术公司的试验将更多5岁以下儿童纳入临床试验,198198彩注册彩注册正规网址是什,这也将提供更多的数据。
例如,自从3-microgram剂量只有有效的孩子年龄在6个月的两年,但在2到5岁的儿童,审判可能所有的参与者5岁以下划分为不同年龄子组和测试不同剂量在每个子集,每个报告。
这篇论文提出了另一种增加可得性的方法,即通过FDA扩大接种计划,使高危儿童可以接种疫苗。
Fatima Khan在change.org网站上向FDA药物评估与研究中心主任珍妮特·伍德考克(Janet Woodcock)博士提交了一份请愿书,称:“我们是5岁以下儿童的父母、照顾者和至爱之人,我们迫切要求你们为这一年龄组提供拯救生命的COVID-19疫苗。”
“我们许多人的孩子太小,不记得大流行之前的生活。我们生了孩子,抚养了新生儿,照顾了蹒跚学步的孩子和学龄前儿童,同时努力在孩子的身心健康之间达到不可能的平衡。”